انواع پیوند های شیمیایی
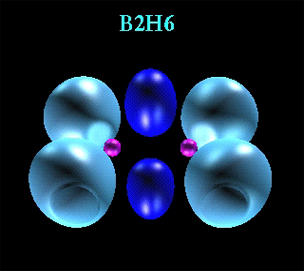
پیوند کووالانسی
در مولکول هیدروژن ، اتمها ، الکترون به اشتراک میگذارند و با استفاده از مدل بور ، الکترونهای مشترک بر روی مدار خارجی هر دو اتم گردش میکنند. به بیان دیگر ، ابر الکترونی تحت تاثیر جاذبه دو هسته قرار دارد و تراکم ابر الکترونی در فاصله دو هسته از جاهای دیگر بیشتر است. چنین پیوندی پیوند کووالانسینامیده میشود.
پیوند کووالانسی بین دو اتم هیدروژن از همپوشانی اوربیتال s بوجود میآید و مولکول حاصل بیضوی است که هستههای دو اتم در دو کانون آن قرار دارند و تراکم ابر الکترونی در بین دو هسته زیاد و در اطراف هستهها کمتر است. در نتیجه تشکیل پیوند ، اوربیتالهای اتمی به اوربیتال مولکولی تبدیل میشوند. اوربیتالهای مولکولی حاصل از تشکیل پیوند میان دو اتم هیدروژن بیضوی است که تراکم ابر الکترونی بر روی خط واصل بین هستههای آن از جاهای دیگر بیشتر است. این شکل اوربیتال مولکولی اوربیتال مولکولی سیگما یا پیوند سیگما نامیده میشود.
در نوع دیگر از اوربیتالهای مولکولی ، نه تنها سطح انرژی پائین نمیآید و انرژی آزاد نمیشود، بلکه سطح انرژی از اتمهای اولیه نیز بالاتر است، این اوربیتال را نمیتوان اوربیتال پیوندی نامید، بلکه یک اوربیتالی ضد پیوندی است و بصورت 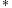 نشان داده میشود.
نشان داده میشود.
هرچه در یک مولکول ، تعداد اوربیتالهای پیوندی اشغال شده بیشتر باشد، مولکول پایدارتر است، ولی هر گاه تعداد اوربیتالهای پیوندی و ضد پیوندی برابر باشد، دو اتم از یکدیگر جدا میمانند و بین آنها پیوندی تشکیل نمیشود. تعداد پیوند میان دو اتم برابر نصف تعداد الکترونهای موجود در اوربیتالهای پیوندی منهای نصف تعداد الکترونهای موجود در اوربیتالهای ضد پیوندی است.
-
پیوند اکسیژن با هیدروژن :
اکسیژن ، دو اوربیتال تک الکترونی دارد. هر گاه یک اتم اکسیژن و یک اتم هیدروژن به یکدیگر نزدیک شوند، امکان جاذبه بر دافعه وجود دارد و در این صورت پیوند تشکیل میشود. در این مجموعه ، هیدروژن به آرایش گاز بیاثر هلیم رسیده است، ولی اکسیژن در خارجیترین سطح انرژی خود دارای هفت الکترون شده و هنوز به آرایش گاز بیاثر نرسیده است.
آرایش الکترونی اکسیژن پس از تشکیل یک پیوند با یک هیدروژن مشابه آرایش الکترونی فلوئور شده است. بنابراین این مجموعه میتواند به همان راههایی که فلوئور آرایش الکترونی خود را به آرایش الکترونی گاز بیاثر رساند، آرایش الکترونی خود را کامل کند. یکی از راههای رسیدن به آرایش الکترونی گاز بیاثر آن است که با یک اتم هیدروژن دیگر پیوند برقرار کند و مولکول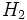 O را پدید آورد.
O را پدید آورد.
پیوند داتیو
اتم نیتروژن با سه اتم هیدروژن ، پیوند کووالانسی معمولی تشکیل میدهد و به آرایش الکترونی گاز بیاثر میرسد. پس از این عمل ، برای نیتروژن یک جفت الکترون غیر پیوندی باقی میماند که میتواند آن را بصورت داتیو در اختیار اتمهایی که به آن نیاز دارند، قرار دهد. از سوی دیگر ، اتم هیدروژن که یک اتم الکترون در اوربیتال 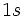 آن موجود است، هر گاه این الکترون را از دست بدهد، به یون
آن موجود است، هر گاه این الکترون را از دست بدهد، به یون  تبدیل میشود که اوربیتال
تبدیل میشود که اوربیتال 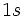 آن خالی است.
آن خالی است.
حال هرگاه این یون به مولکول آمونیاک نزدیک شود، با آن پیوند داتیو برقرار میکند و خود را به آرایش الکترونی گاز بیاثر میرساند:  این مجموعه کهیون آمونیوم نامیده میشود، در بسیاری از ترکیبات مانند کلرید آمونیوم
این مجموعه کهیون آمونیوم نامیده میشود، در بسیاری از ترکیبات مانند کلرید آمونیوم 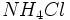 و هیدروکسید آمونیوم
و هیدروکسید آمونیوم  وجود دارد.
وجود دارد.
اندازه گیریهای انجام شده نشان میدهد که انرژی و طول هر چهار پیوند نیتروژن _ هیدروژن در یون آمونیوم کاملا یکسان است. این امر منطقی نیز به نظر میرسد، زیرا پیوند داتیو نیز مانند پیوند کووالانسی معمولی یک جفت الکترون است که بین هسته اتم نیتروژن و هسته اتم هیدروژن قرار گرفته است.
هچنین  میتواند با یون
میتواند با یون 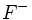 یون
یون  تشکیل دهد که در آن هر چهار پیوند از نظر طول و انرژی یکسان هستند. کلرید آلومینیوم نیز با یون
تشکیل دهد که در آن هر چهار پیوند از نظر طول و انرژی یکسان هستند. کلرید آلومینیوم نیز با یون 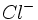 ترکیب میشود و یون
ترکیب میشود و یون  تولید میکند که در آن هر چهار پیوند AL - Cl از نظر طول و انرژی یکسان هستند.
تولید میکند که در آن هر چهار پیوند AL - Cl از نظر طول و انرژی یکسان هستند. 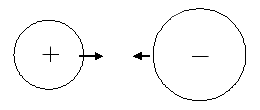
پیوند الکترووالانسی (یونی)
در اتم لیتیم ، 2 الکترون وجود دارد که یک الکترون ، در لایه والانس آن قرار دارد. به هنگام تشکیل پیوند ، چون این اتم در دومین سطح انرژی دارای جفت الکترون غیر پیوندی نیست و تفاوت سطح انرژی اول و دوم نیز بسیار زیاد است، نمیتواند الکترون خود را برانگیخته کند. بنابراین در خارجیترین سطح انرژی ، تنها یک الکترون خواهد داشت. هرگاه این اتم بخواهد پیوند کووالانسی تشکیل دهد، باید یک اتم تک الکترونی دیگر مانند فلوئور پیوند تشکیل دهد و  را تولید کند.
را تولید کند.
واقعیت آن است که از پیوند بین لیتیم و فلوئور ، فلورید لیتیم  پدید میآید، ولی هرگاه بخواهیم این دو اتم را از نظر آرایش الکترونی بررسی کنیم، مشاهده خواهیم کرد که اتم فلوئور با اشتراک گذاشتن الکترون ، ممکن است به آرایش الکترونی گاز بیاثر برسد، ولی لیتیم آرایش الکترونی گاز بیاثر پیدا نکرده است.
پدید میآید، ولی هرگاه بخواهیم این دو اتم را از نظر آرایش الکترونی بررسی کنیم، مشاهده خواهیم کرد که اتم فلوئور با اشتراک گذاشتن الکترون ، ممکن است به آرایش الکترونی گاز بیاثر برسد، ولی لیتیم آرایش الکترونی گاز بیاثر پیدا نکرده است.
لیتیم هر گاه بخواهد به آرایش الکترونی گاز بیاثر بعد از خود برسد، باید روی هم رفته هفت الکترون بگیرد که اگر بخواهد این هفت الکترون را با پیوند کووالانسی بدست آورد، خود نیز باید هفت الکترون در خارجیترین سطح انرژی خود داشته باشد که این کار به هیچ وجه امکان پذیر نیست.
ولی هر گاه این عنصر بخواهد آرایش الکترونی گاز بیاثر قبل خود را پیدا کند، کافی است که یک الکترون موجود در اوربیتال 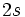 خود را از دست بدهد تا آرایش الکترونی آن به صورت
خود را از دست بدهد تا آرایش الکترونی آن به صورت 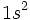 در آید و آرایش الکترونی گاز بیاثر هلیم پیدا کند. یعنی اتم لیتیم به یون
در آید و آرایش الکترونی گاز بیاثر هلیم پیدا کند. یعنی اتم لیتیم به یون  تبدیل میشود و به آرایش گاز هلیم میرسد.
تبدیل میشود و به آرایش گاز هلیم میرسد.
اتم فلوئور نیز میتواند با گرفتن یک الکترون و تبدیل شدن به یون 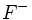 خود را به آرایش الکترونی گاز بی اثر نئون برساند. یعنی به هنگام تشکیل پیوند بین لیتیم و فلوئور ، لیتیم یک الکترون به فلوئور میدهد و با این عمل هر دو به آرایش الکترونی گاز بیاثر میرسند. به این ترتیب اتم فلوئور به یون منفی (آنیون) و اتم لیتیم به یون مثبت (کاتیون) تبدیل میشود. این نوع پیوند را پیوند الکترووالانسی یا یونی مینامند که بین یک فلز و یک غیرفلز رخ میدهد.
خود را به آرایش الکترونی گاز بی اثر نئون برساند. یعنی به هنگام تشکیل پیوند بین لیتیم و فلوئور ، لیتیم یک الکترون به فلوئور میدهد و با این عمل هر دو به آرایش الکترونی گاز بیاثر میرسند. به این ترتیب اتم فلوئور به یون منفی (آنیون) و اتم لیتیم به یون مثبت (کاتیون) تبدیل میشود. این نوع پیوند را پیوند الکترووالانسی یا یونی مینامند که بین یک فلز و یک غیرفلز رخ میدهد.

البته اگه در کنار این وبلاگ کانال تلگرام هم راه بندازین عالی تر هم میشه
با تشکر